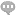药物的杂质检查是保证药品质量的重要环节。杂质可能来源于药物的生产过程、储存过程或药物本身的降解产物。一般杂质检查包括氯化物、硫酸盐、重金属、砷盐等检查。以重金属检查为例,常用的方法是硫代乙酰胺法。在弱酸性(pH3.5)条件下,硫代乙酰胺水解产生硫化氢,与药物中的重金属离子(如铅、汞等)反应生成有色硫化物沉淀。通过与标准铅溶液产生的沉淀颜色深浅比较,判断药物中的重金属含量是否符合规定。特殊杂质检查则是针对特定药物中可能存在的特殊杂质。例如,在阿司匹林的生产过程中,可能会产生水杨酸杂质。水杨酸可与铁盐试剂反应生成紫堇色配合物,通过比色法可以检测阿司匹林中水杨酸的含量。杂质检查实验需要严格控制实验条件,确保结果的准确性。采用的分析方法要具有足够的灵敏度和专属性,能够准确地检测出杂质的种类和含量。对于超过规定限量的杂质,药物将被判定为不合格产品,不能用于临床。石蜡包埋与切片服务,确保样本质量。上海实验报告

网状纤维染色是一种特殊的病理染色实验,主要用于显示组织中的网状纤维结构。网状纤维是一种纤细的纤维,主要由III型胶原蛋白组成。在某些病理情况下,网状纤维的分布和数量会发生变化。例如在肝脏疾病中,肝纤维化时网状纤维会大量增生。在网状纤维染色中,常用的方法是Gomori银染法。其原理是网状纤维具有还原银离子的能力,使银离子还原成金属银沉积在网状纤维上,从而使其被染成黑色。染色过程中,组织切片要经过固定、清洗等常规步骤后,进入银染液。银染液的配制和使用条件需要严格控制,例如银染液的浓度、反应的温度和时间等。如果银染液浓度过高或者反应时间过长,可能会导致背景染色过深,影响网状纤维的观察;反之,如果浓度过低或时间过短,则网状纤维染色不明显。网状纤维染色后的切片有助于病理学家判断组织的结构完整性,在**的浸润和转移研究中,网状纤维的分布可以反映肿瘤细胞与周围组织的关系;在肝脏、肾脏等***疾病的研究中,也能提供关于***纤维化程度等重要信息。浙江细胞实验报告多重荧光染色实验,满足复杂研究需求。

免疫荧光染色是病理实验中一种重要的检测技术。它基于抗原-抗体特异性结合原理,与免疫组织化学染色类似,但标记物为荧光素。首先,组织切片或细胞涂片要进行固定、通透处理,使抗体能够进入细胞内与抗原结合。然后将切片与一抗孵育,一抗与目标抗原特异性结合。孵育后洗涤切片,再与带有荧光标记的二抗孵育。常用的荧光素有异硫氰酸荧光素(FITC),发出绿色荧光;四甲基罗丹明异硫氰酸酯(TRITC),发出红色荧光等。在荧光显微镜下,可以观察到带有荧光标记的抗原分布情况。
细胞免疫荧光实验是在细胞水平上检测特定蛋白的定位和表达情况的方法。首先,将细胞接种在盖玻片上培养。固定细胞是关键的第一步,可以使用多聚甲醛等固定剂,它能保持细胞的形态结构并固定细胞内的蛋白。然后进行通透处理,如用TritonX-100,使抗体能够进入细胞内与目标蛋白结合。接着,将细胞与特异性的一抗孵育,一抗与目标蛋白特异性结合。之后用带有荧光标记的二抗孵育,二抗识别一抗并带有如异硫氰酸荧光素(FITC)或四甲基罗丹明异硫氰酸酯(TRITC)等荧光标记。在荧光显微镜下,可以观察到带有荧光标记的蛋白在细胞内的分布情况。例如,在研究细胞骨架蛋白时,可以看到微管蛋白(用一种荧光标记)和肌动蛋白(用另一种荧光标记)在细胞内的不同分布模式,从而了解细胞的结构和形态维持机制。病理样本库建设与管理,确保样本安全。

兔子在眼科研究中意义非凡。兔子的眼球结构与人类较为相似,这为眼科研究提供了良好的动物模型。在研究眼部疾病方面,例如青光眼。可以通过手术或者药物诱导的方式使兔子患上青光眼,模拟人类青光眼患者眼压升高、视神经损伤的症状。然后研究人员可以测量兔子眼压的变化,观察视神经**的形态改变以及视网膜神经节细胞的损伤情况。通过对兔子青光眼模型的研究,可以深入探讨青光眼的发病机制,如眼内房水循环的异常是如何导致眼压升高的。在眼部药物研发中,兔子也是理想的实验对象。当研发一种新的眼药水时,将眼药水滴入兔子的眼睛,然后观察药物在兔子眼内的吸收情况、药物对眼部组织的刺激性以及药物的***效果等。例如,检测药物是否能够降低眼压、改善视网膜功能等。然而,兔子的眼部结构和人类也并非完全相同。兔子的眼睛相对较大,眼内的一些生理参数(如房水生成率等)与人类存在差异。所以在将兔子实验结果应用于人类眼科疾病的诊断和***时,还需要综合考虑这些因素。病理切片染色实验耗材采购,降低成本。浙江细胞实验报告
病理实验技术交流平台,促进合作。上海实验报告
药物的药理活性筛选实验是新药研发的重要步骤。这个实验旨在从众多的化合物中筛选出具有潜在药理活性的物质。首先,要建立合适的药理模型。对于***药物的筛选,可以采用小鼠耳肿胀模型。通过给小鼠耳部涂抹致炎物质(如二甲苯)引起炎症反应,然后将待测化合物给予小鼠,观察耳部肿胀程度的变化。如果化合物能够减轻耳部肿胀,就可能具有***活性。对于抗**药物的筛选,可以采用体外细胞实验和体内动物模型相结合的方式。在体外,利用肿瘤细胞系(如人肺*细胞A519),将待测化合物与肿瘤细胞共同培养,通过检测细胞的增殖、凋亡等指标来初步判断化合物的抗**活性。在体内,将肿瘤细胞接种到小鼠体内形成**模型,再给予待测化合物,观察**的生长抑制情况、小鼠的生存状态等。在筛选过程中,要设置阳性对照组(已知具有药理活性的药物)和阴性对照组(溶剂或无药理活性的物质)。通过对比分析,确定待测化合物是否具有药理活性以及活性的强弱。这个实验为进一步的药物研发提供了基础,能够缩小研究范围,提高新药研发的效率。上海实验报告
文章来源地址: http://yyby.huanbaojgsb.chanpin818.com/yyxmhz/deta_27136424.html
免责声明: 本页面所展现的信息及其他相关推荐信息,均来源于其对应的用户,本网对此不承担任何保证责任。如涉及作品内容、 版权和其他问题,请及时与本网联系,我们将核实后进行删除,本网站对此声明具有最终解释权。



 [VIP第1年] 指数:3
[VIP第1年] 指数:3